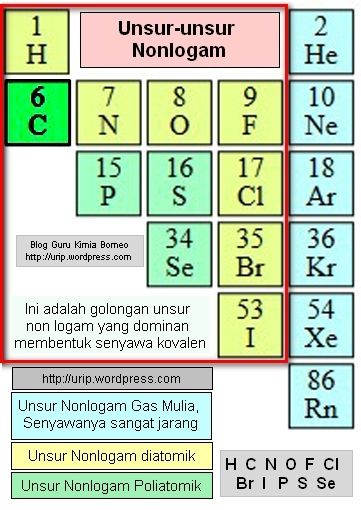
Biasanya senyawa kovalen mampu mendidih di bawah 200 C sedangkan senyawa ion biasanya bisa mendidih di atas suhu 900 C. Berikut adalah perbedaan antara ikatan kovalen dan ikatan Ion.

Tuliskan Dalam Bentuk Tabel Minimal 8 Senyawa Ion Beserta Titik Leleh Dan Titik Didih Brainly Co Id
Pada ikatan ion terjadi gaya elektrostatik gaya Coulomb sehingga pada senyawa ion diperlukan energi lebih besar untuk mengalahkan gaya tersebut.
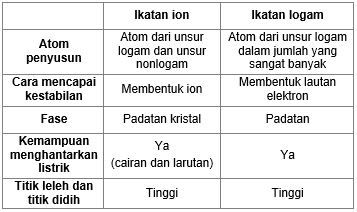
. Ikatan ion ikatan kovalen Otosection Home. Akibatnya titik lebur dan titik didih senyawa ion lebih tinggi dibandingkan dengan senyawa kovalen. -- Ikatan Kimia Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya.
Pada suhu kamar berbentuk gas ada juga yang berwujud cair dan padat. Perbandingan sifat senyawa kovalen dan senyawa ion. Brom karbon dioksida Heksana Amoia dan etil alohol merupakan contoh dari senyawa semnyawa kovalen.
Jadi perbedaan sifat senyawa ionik dan kovalen dapat dilihat dari wujudnya titik didih dan titik leleh kelarutan dan. Pada Ikatan Kovalen 1Bentuk Senyawa yang dapat terjadi. Bentuk senyawa ion berupa zat padat pada suhu kamar.
Berikut ini ringkasan singkat perbedaan antara ikatan ion dan kovalen sifat-sifatnya dan cara mengenalinya. Pada suhu kamar berbentuk lunak. Memiliki titik didih dan titik leleh yang relatif rendah.
Urea mempunyai titik leleh pada kisaran antara 30 95 naftalena antara 30 -61 NaCl antara 85 100 KI antara 62 100 MgSO4 antara 30. Ikatan yang terjadi antar-molekul CH4 adalah ikatan. Titik didih cuka 119C dan garam dapur 1517C.
Hal ini disebabkan oleh cara pembentukan ikatan yang berbeda. Perbandingan beberapa sifat senyawa kovalen dan ion. Ikatan kovalen yang mengikat antara atom hidrogen dan atom oksigen dalam molekul.
Berdasarkan sifat periodik unsur-unsur golongan VIA H2O seharusnya memiliki titik didih yang lebih kecil dibandingkan titik didih H2S. Banyak perbedaan yang dapat diketahui antara senyawa ionik dan kovalen berdasarkan sifat makroskopisnya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih. Jika ditinjau dari sifat fisik kedua senyawa ini perbedaannya adalah sebagai berikut.
Sifat fisis senyawa ion umumnya berbeda dengan senyawa kovalen. Perbedaan selanjutnya yang akan sobat pelajari di kelas X ini adalah daya. Tidak mudah patah dan mudah dibentuk.
Mereka juga memiliki sifatnya sendiri sehingga bisa menjadi pembeda dengan senyawa yang lain. 2 Umumnya cairan atau gas pada Semuanya dalah padatan pada suhu. Dalam keadaan cair atau dalam larutan senyawa ionik dapat menghantarkan arus listrik karena kation dan anion dapat bergerak bebas.
Selanjutnya senyawa ionik memiliki titik didih dan titik leleh yang relatif tinggi karena ikatan ion yang terbentuk sangat kuat. Titit leleh dan titik didih senyawa kovalen cenderung lebih rendah daripada senyawa ion. Oleh karena itu pola ikatan mereka dapat.
Perbedaan antara mereka ada hubungannya dengan seberapa sama atom yang berpartisipasi dalam ikatan berbagi elektron mereka. 6Titik Leleh dan Titik Didih Lebih tinggi karena ion-ionnya terikat kuat pada kisi-kisinya sehingga untuk memutuskan ikatan diperlukan energi yang lebih besar. Salah satu perbedaan yang tampak antara senyawa kovalen dan senyawa ion dapat dilihat dari wujudnya yaitu pada suhu kamar atau ruangan senyawa ion dapat berbentuk padat sedangkan senyawa kovalen berbentuk cair atau gasTetapi seperti yang kita ketahui dari percobaan bahwa urea adalah senyawa kovalen yang.
Senyawa ionik adalah senyawa yang terbentuk karena adanya ikatan ion sedangkan senyawa kovalen terbentuk karena adanya ikatan kovalen. Alasan utama perbedaan ini adalah perbedaan dalam pola ikatan mereka. Senyawa ion memiliki titik didih yang rendah sedangkan senyawa kovalen memiliki titik didih yang tinggi.
Bentuknya keras namun rapuh. Namun kekuatan ikatan kovalen lebih lemah dibandingkan ikatan ion. Dapat menghantarkan listrik dan panas.
Pada hasil pengamatan terhadap pengujian senyawa ion dan kovalen dengan memanaskan senyawa-senyawa tersebut didapatkan perbedaan titik leleh antara dua senyawa tersebut. Padatan wujud ini tidak dap. -- Perbedaan Senyawa Ion Dan Kovalen Brainly Mazalie Perbedaan senyawa ionik dan senyawa kovalen.
Titik didih dan titik leleh tinggi. Alasan utama perbedaan ini adalah perbedaan pola ikatannya. Perbedaan Kunci - Senyawa Ionic vs Kovalen.
Akibatnya senyawa ion memiliki titik didih dan titik leleh. Oleh karena itu mereka pola ikatan dapat dianggap sebagaiperbedaan utama antarasenyawa ionik dan. Pada senyawa CH4 perbedaan keelektronegatifan C dan H sangat kecil.
Titik didih dan titik leleh yang tinggi. Sifat-sifat senyawa kovalen adalah. Dua jenis ikatan adalah ikatan ionik dan ikatan kovalen.
Namun masih banyak lagi perbedan antara senyawa yang. Begitu juga dengan senyawa ion dan kovalen. Nahh demikian perbedaan sifat fisik dari Senyawa Ion Senyawa Kovalen dan Logam ya otakers Semoga bermanfaat yah.
Ikatan ion Dalam ikatan ion satu atom pada dasarnya. Ringkasan perbedaan Ikatan ion dan kovalen. Suatu molekul atau senyawa dibuat ketika dua atau lebih atom membentuk ikatan kimia yang menghubungkannya bersama.
Sifat senyawa ion maupun sifat senyawa kovalen dapat kita jabarkan sebagai berikut. Sebagai contoh Air H2O merupakan senyawa kovalen. Juga senyawa kovalen dapat larut dalam air tetapi tidak berdisosiasi menjadi ion.
No Senyawa kovalen Senyawa ion 1 Kebanyakan menunjukkan titik Kebanyakan menunjukkan titik leleh rendah. Untuk mengetahui perbedaan senyawa ion dan senyawa kovalen. Senyawa yang mengandung ikatan ionik dapat bertindak sebagai konduktor yang baik.
Senyawa ion dan senyawa kovalen sama-sama memiliki ikatan yang kuat. Berikut ini akan dibahas mengenai perbedaan sifat fisika senyawa ion dan senyawa kovalen yang meliputi titik leleh dan titik didih kemudahan menguap volatile daya hantar listrik dan kelarutan. Alasan untuk fakta ini adalah bahwa senyawa ionik memerlukan sejumlah besar energi untuk memutuskan ikatan ionik mereka dan memisahkan gaya tarik muatan positif dan negatif.
Leleh tinggi 350oC sering sampai 1000oC. Ikatan kovalen merupakan ikatan yang terjadi antara dua atom dengan pemakaian bersama sama. Mudah larut dalam pelarut polar.
Senyawa ionik memiliki titik leleh dan titik didih yang tinggi sedangkan senyawa kovalen memiliki titik leleh dan titik didih yang relatif rendah. Pada umumnya senyawa kovalen mempunyai titik didih yang rendah rata-rata di bawah suhu 200 0C. 213 Sifat Sifat Senyawa Kovalen.
Banyak perbedaan yang dapat dicatat antara senyawa ionik dan kovalen berdasarkan sifat makroskopiknya seperti kelarutan dalam air konduktivitas listrik titik leleh dan titik didih. Berikut ini akan dibahas beberapa perbedaan sifat fisik senyawa ion dan senyawa kovalen seperti kemudahan menguap volatile daya hantar listrik. Pada umumnya senyawa ion larut dalam pelarut polar seperti air dan ammonia karena sebagian molekul pelarut menghadapkan kutub negatifnya ke ion positif dan sebagian lagi menghadapkan kutub positifnya ke ion negatif.
Van der Waals E. Senyawa kovalen polar hanya dapat menghantarkan listrik dalam larutan dan senyawa kovalen nonpolar tidak dapat menghantarkan listrik. Pada kasus tersebut cuka mudah menguap dibandingkan garam dapur.
Lakukan Analisis Apakah Perbedaan Dan Persamaan Da

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id

Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

10 Perbedaan Senyawa Ion Dan Senyawa Kovalen

Buat Yang Kelas 10 Yuk Mengenal Ikatan Ikatan Kimia Dalam Atom

Ciri Ciri Dari Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Sebutkan 5 Contoh Perbedaan Antara Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

Sebutkan Perbedaan Sifat Antara Senyawa Ion Dengan Senyawa Kovalen Brainly Co Id

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube
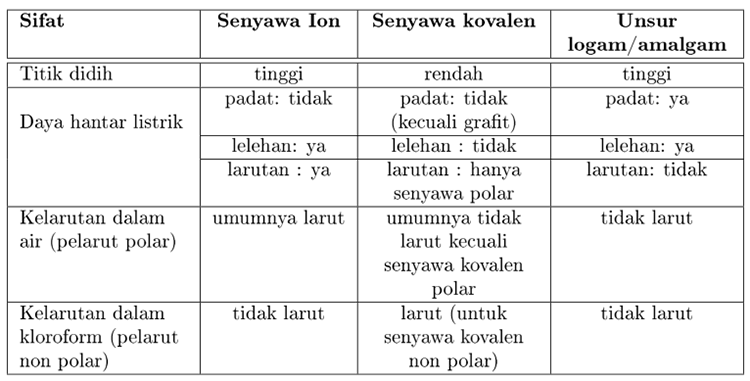
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College

Perbedaan Senyawa Ion Dan Senyawa Kovalen Youtube

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Pengertian Sifat Dan Contoh Dari Senyawa Ion Panduan Kimia Riset

Pengertian Senyawa Kovalen Contoh Sifat Dan Rumus Senyawa

Perbedaan Senyawa Ion Senyawa Kovalen Dan Logam Utakatikotak Com
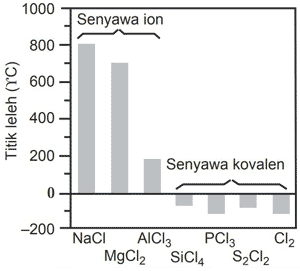
Perbedaan Senyawa Ion Dan Kovalen
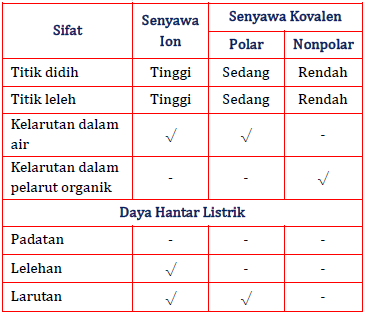
Diketahui Data Fisik Dua Buah Senyawa Sebagai Beri